В статье приведены данные об исследованиях, способствующих совершенствованию дифференциальной диагностики Т- и В-клеточных лимфом кожи, в том числе с крупнобляшечным парапсориазом, Т- и В-клеточными псевдолимфомами кожи, а также о частоте их трансформации в злокачественные лимфомы кожи. У 101 пациента проведено обследование методом полимеразной цепной реакции с целью определения Т- и В-клеточной клональности лимфоцитов по генам g- и β-цепей Т-клеточного рецептора и генам тяжелой цепи иммуноглобулина. У пациентов с Т-клеточными лимфомами кожи моноклональность определялась в 40 из 46 случаев, с В-клеточными лимфомами кожи — в 3 из 4 случаев. Также моноклональность была выявлена в 1 из 14 случаев крупнобляшечного парапсориазам и в 1 из 2 случаев Т-клеточной псевдолимфомы кожи. Во всех 24 случаях хронических доброкачественных дерматозов, 5 случаях мелкобляшечного парапсориаза и 10 биоптатах кожи от здоровых доноров была выявлена поликлональность лимфоцитов. Таким образом, полученные результаты позволяют считать данный метод важным дополнением в диагностике лимфопролиферативных заболеваний кожи.
Как известно, молекулярно-генетические методы определения клональности лимфоцитов, основанные на применении полимеразной цепной реакции (ПЦ Р), повышают точность выявления злокачественных лимфом кожи (ЗЛК) [1]. Однако используемый ранее полиакриламидный гель-электрофорез был менее информативным при ЗЛК [2, 3] по сравнению с разработанным и используемым в настоящее время методом фрагментного анализа (the automated high-resolution PCR fragment analysis). Высокая чувствительность данного метода основывается на возможности дифференцировать нуклеотидные последовательности с точностью до одного нуклеотида [2].
Метод фрагментного анализа основан на разделении меченных флюоресцентным красителем ПЦР-продуктов в капиллярах, заполненных гелем. Для исследования используется автоматический анализатор нуклеиновых кислот. Флюоресцентный сигнал, испускаемый ПЦР-продуктом, фиксируется в виде пика определенной высоты и площади в зависимости от интенсивности свечения [4].
При ПЦР-анализе исследуется уникальная для каждого Т- и В-лимфоцита область соединения V-D-J сегментов (CDR3 области) генов гамма- и бета-цепей Т-клеточных рецепторов лимфоцитов (TCRγ и TCRβ), а также генов тяжелой цепи иммуноглобулинов (IgH). При появлении клона лимфоцитов, если перестройка прошла на одной хромосоме (моноаллельная перестройка), среди амплификатов будет доминировать один ПЦР-продукт, если перестройка прошла на двух гомологичных хромосомах (биаллельная перестройка) — два ПЦР-продукта [5].
Клональность лимфоцитов определяется при наличии 1—10% опухолевых лимфоцитов в образце, что позволяет выявлять ее не только в биоптатах кожи, но и в образцах крови [6, 7].
Основным показанием к определению клональности Т- и В-лимфоцитов является дифференциальная диагностика опухолевой и реактивной пролиферации лимфоцитов [3, 8]. Определение моноклонального типа пролиферации свидетельствует о злокачественном характере болезни. Однако иногда моноклональность лимфоцитов может выявляться при различных хронических воспалительных дерматозах (ХВД), таких как псориаз, экзема, атопический дерматит [9—11], инфекционных воспалительных процессах (инфекционный мононуклеоз) [12] или системных заболеваниях соединительной ткани (системная склеродермия, системная красная волчанка и т. д.). При этих заболеваниях высота доминирующих пиков, обозначающих клоны лимфоцитов (по данным фореграмм фрагментного анализа), достоверно ниже, чем при ЗЛК [13]. Поликлональный тип пролифераций выявляется при доброкачественных реактивных лимфопролиферативных процессах и ХВД. При ЗЛК, даже подтвержденных гистологически, возможно отсутствие моноклональности лимфоцитов инфильтрата, что связано с неравномерным распределением лимфоцитов в коже. Это, в частности, наблюдается при эритродермии у больных грибовидным микозом, при котором воспалительный компонент доминирует над пролиферативным, а также при незначительном количестве опухолевых лимфоцитов в биоптате коже на начальных стадиях лимфомы кожи [14, 15]. Следует отметить, что моноклональность опухолевых лимфоцитов может иметь место не только в биоптате пораженной кожи, но и в крови этого же пациента в 15% случаев на ранних стадиях и 63% на поздних стадиях грибовидного микоза [16]. При этом эффективность ранней диагностики ЗЛК повышается путем одновременного гистологического и молекулярно-генетического исследования двух биоптатов пораженной кожи в совокупности с образцом крови пациента.
С учетом вышесказанного целью настоящего исследования явилось совершенствование дифференциальной диагностики Т- и В-клеточных лимфом кожи (ТКЛК и ВКЛК) с крупнобляшечным парапсориазом (КБП), Т- и В-клеточными псевдолимфомами (ТПЛК и ВПЛК) кожи, с ХВД, а также уточнение частоты их трансформации в ЗЛК.
Материал и методы
Метод фрагментного анализа для определения клональности лимфоцитов был применен нами при обследовании 101 пациента (66 мужчин и 35 женщин) с патологическим процессом, требующим дифференциальной диагностики с ТКЛК и ВКЛК. Возраст пациентов варьировал от 27 до 87 лет (средний возраст 57 лет). У 46 из них был гистологически установлен диагноз ТКЛК, у 4 — ВКЛК, у 19 — парапсориаз, у 8 — псевдолимфомы кожи. В группу больных с ХВД, схожими по ряду клинических симптомов с ТКЛК, было включено 24 пациента с гистологически установленным диагнозом хронического воспалительного процесса (табл. 1).
Все пациенты были обследованы в отделении дерматоонкологии и дерматовенерологии и отделении патоморфологии ГУ МОНИКИ им. М.Ф. Владимирского. Молекулярные методы определения клональности лимфоцитов проводились в лаборатории молекулярной гематологии ГНЦ РАМН. Диагноз лимфомы кожи устанавливали в соответствии с международной классификацией лимфом кожи WHO /EORTC (2005 г.) [17]. Объектом исследования являлись биоптаты пораженной кожи, у 3 больных помимо двух биоптатов исследовали на клональность лимфоцитов образцы периферической крови.
В качестве положительного (моноклонального) контроля использовали клеточную линию Jurkat (линия клеток Т-лимфобластного острого лейкоза), имеющую биаллельную перестройку гамма-цепи Т-клеточного рецептора, которая выявляется с Vγ1—8 и Vγ11 праймерами. В качестве поликлонального контроля использовали мононуклеары периферической крови здоровых доноров и образцы кожи, полученные в ходе пластических операций у здоровых людей.
| Нозологическая форма | Число больных | Пределы возраста, лет | Мужчины/женщины |
|---|---|---|---|
| Т-клеточные лимфомы кожи (n=46) | |||
| Грибовидный микоз | 40 | 60,7 | 23/17 |
| Синдром Сезари | 2 | 78 | 2/0 |
| Первичная кожная CD30+ анапластическая крупноклеточная лимфома | 3 | 72,7 | 1/2 |
| Первичная кожная агрессивная лимфома кожи | 1 | 76 | 0/1 |
| В-клеточные лимфомы кожи (n=4) | |||
| Первичная кожная диффузная В-клеточная крупноклеточная лимфома типа нижних конечностей | 1 | 70 | 0/1 |
| Первичная кожная лимфома из клеток фолликулярного центра | 2 | 71,5 | 1/1 |
| Первичная кожная лимфома маргинальной зоны | 1 | 76 | 1/0 |
| Парапсориаз (n=19) | |||
| Крупнобляшечный | 14 | 42,2 | 8/6 |
| Мелкобляшечный | 5 | 46,3 | 4/1 |
| Т-клеточные псевдолимфомы кожи (n=2) | |||
| Актинический ретикулоид | 1 | 65 | 1/0 |
| Т-клеточная лимфоидная гиперплазия | 1 | 44 | 1/0 |
| В-клеточные псевдолимфомы кожи (n=6) | |||
| Лимфоматоидная реакция на укусы насекомых | 2 | 64,5 | 0/2 |
| Постскабиозная гиперплазия | 3 | 65,7 | 1/2 |
| Лимфоцитома | 1 | 49 | 0/1 |
| Хронические воспалительные дерматозы (n=24) | |||
| Атопический дерматит | 5 | 33,8 | 3/2 |
| Псориаз | 8 | 55,2 | 7/1 |
| Экзема | 6 | 54,5 | 2/4 |
| Красный плоский лишай | 2 | 38 | 1/1 |
| Склеродермия | 2 | 42 | 0/2 |
| Розовые угри | 1 | 31 | 0/1 |
Выделение ДНК
Мононуклеары из периферической крови выделяли в градиенте плотности фиколла (плотность 1,077 г/см3) стандартным методом. ДНК выделяли из мононуклеаров периферической крови с помощью набора Wizard genomic DNA purification system (Ргоmеgа, США), из свежей или замороженной ткани (кожи и крови) стандартным методом — обработкой протеиназой К с последующей очисткой в феноле и хлороформе и осаждением в трех объемах 96% этилового спирта с раствором аммония ацетата в конечной концентрации 1М. Концентрацию выделенной ДНК проверяли на спектрофотометре Beckman DU-64.
Анализ В-клеточной клональности по генам IgH и Т-клеточной клональности по генам TCRγ и TCRβ
Определение В-клеточной клональности лимфоцитов проводили на основе анализа перестроек вариабельного региона генов тяжелой цепи иммуноглобулина, T-клеточной клональности лимфоцитов — на основе перестроек генов γ- и β-цепи Т-клеточного рецептора. Определение клональности лимфоцитов проводили методом ПЦР и методом фрагментного анализа. Для определения B-клеточной клональности лимфоцитов использовали смесь праймеров к фракциям FR1, FR2, FR3 вариабельного региона генов IgH и меченный флюоресцентной краской консенсусный праймер к J-региону IgH [18].
Для мультиплексной ПЦР-генов TCRγ применяли два набора праймеров: 1) смесь праймеров Tγ [18], 2) смесь праймеров Tγγ [19]. Для мультиплексной ПЦР генов TCR β применяли смесь праймеров Tβ [18]. Все праймеры для определения T-клеточной клональности лимфоцитов — смесь прямых праймеров к V генам TCR и меченных флюоресцентной краской обратных праймеров к J генам TCR. ПЦР проводили на автоматическом термоциклере DNAEngine (BioRad). Реакционная смесь в конечном объеме 20 мкл включала: 200 нг ДНК, 10 мкл 2 X смеси для ПЦР (PCR Master Mix Promega), 5 пмоль каждого праймера. Условия ПЦР: предварительная денатурация 95 °С (5 мин), 35 циклов ПЦР для IgH и TCRγ и 40 циклов для TCRβ — 95 °С (35 с.), 60 °С (35 с.), 72 °С (35 с.), окончательная пролонгация 72 °С (10 мин.). Результаты реакции выявляли в 2% агарозном геле, окрашенном бромидом этидия. При успешной ПЦР проводили очистку ПЦР продуктов и фрагментный анализ.
Очистка ПЦР-продуктов и фрагментный анализ амплификатов
Для очистки ПЦР-продуктов в каждую пробирку добавляли по 100 мкл смеси для осаждения ДНК (0,25
объема 10М раствора ацетата аммония, 2–2,5 объема 96% этилового спирта), инкубировали 20 мин. при комнатной температуре, центрифугировали 20 мин. при 13 000 g. Осадок ДНК дважды отмывался 70% спиртом, высушивался при комнатной температуре, разбавлялся дистиллированной водой 30 мкл. Концентрация очищенных продуктов проверялась в 2% агарозном геле, окрашенном бромидом этидия. В за висимости от интенсивности свечения ПЦР-продукты разводились в 10–40 раз. Разведенные продукты смешивались с формамидом (2 мкл продукта, 10 мкл формамида, 0,05 мкл внутреннего стандарта Genescan 500LIZ (Applied Biosystems). Денатурацию ДНК проводили в растворе с низкой ионной силой. 5 мкл ПЦ Р-продукта разводили в 15 мкл LIS-solution (10% раствор сахарозы + 0,01% бромфеноловый синий), полученную смесь инкубировали в течение 5 мин. при температуре 95 °С, а затем быстро охлаждали во льду до 0 °С в течение 10 мин. Затем 10 мкл денатурированного продукта наносили в плашку автоматического секвенатора. Для фрагментного анализа использовали автоматический анализатор нуклеиновых кислот ABI Prism 3130 (Applied Biosystems) и программное обеспечение GeneMapper 4.0 (Applied Biosystems).
Критерии интерпретации результатов
Результат фрагментного анализа был виден как набор пиков в области амплификации Tγ — 90 — 240 п.н., Tγγ — 100 — 260 п.н., Tβ — 200–250 п.н. Отрицательный (поликлональный) результат определяли при наличии множества пиков ПЦР-продукта. Результат считался положительным (моноклональным) при наличии одного или двух четких доминантных пиков ПЦР-продукта (в случае биаллельной реарранжировки). При этом пики ПЦР-продукта должны были преобладать и превышать поликлональный фон более чем в 3 раза. Если имелось более трех четких пиков, то результат оценивался как олигоклональный. При наличии одного или двух четких пиков, которые превышали поликлональный фон в 2–3 раза, результат оценивался как сомнительный моноклональный.
Из 46 больных ТКЛК моноклональность по генам TCRγ была обнаружена у 40 (87%). Из 20 этих же больных по генам TCRβ моноклональность лимфоцитов была обнаружена у 5 (25%). Более подробные данные о выявлении моноклональности лимфоцитов по генам γ- и β-цепей TCR с учетом клинических и иммунофенотипических особенностей лимфом кожи представлены в табл. 2.
| Диагноз | Обследовано (n=46) | Моноклональность по генам TCRγ (n=40) | Моноклональность по генам TCRγ, -β (n=5) | Поликлональность (n=6) |
|---|---|---|---|---|
| Грибовидный микоз | 40 | 34 | 5 | 6 |
| Синдром Сезари | 2 | 2 | 0 | 0 |
| Первичная кожная CD30+ анапластическая крупноклеточная лимфома | 3 | 3 | 0 | 0 |
| Первичная кожная агрессивная лимфома кожи | 1 | 1 | 0 | 0 |
Из 14 больных КБП моноклональность по генам TCRγ была обнаружена у 1 (7%), при мелкобляшечном парапсориазе (МБП) — ни в одном из 5 случаев.
Из 4 больных ВКЛК моноклональность лимфоцитов по генам тяжелой цепи IgH была выявлена у 3 (75%).
Из 2 пациентов с ТПЛК монокональность по генам TCRγ была обнаружена только у 1, а также из 6 больных с ВПЛК моноклональность по генам IgH не была обнаружена ни у одного пациента.
В 24 случаях ХВД в биоптате кожи была выявлена поликлональность по генам TCRγ.
При исследовании 10 биоптатов кожи и образцов периферической крови контрольной группы здоровых доноров была выявлена поликлональность по генам TCRγ.
Из 14 больных КБП моноклональность по генам TCRγ была обнаружена у 1 (7%), при мелкобляшечном парапсориазе (МБП) — ни в одном из 5 случаев. Из 4 больных ВКЛК моноклональность лимфоцитов по генам тяжелой цепи IgH была выявлена у 3 (75%). Из 2 пациентов с ТПЛК монокональность по генам TCRγ была обнаружена только у 1, а также из 6 больных с ВПЛК моноклональность по генам IgH не была обнаружена ни у одного пациента. В 24 случаях ХВД в биоптате кожи была выявлена поликлональность по генам TCRγ. При исследовании 10 биоптатов кожи и образцов периферической крови контрольной группы здоровых доноров была выявлена поликлональность по генам TCRγ.
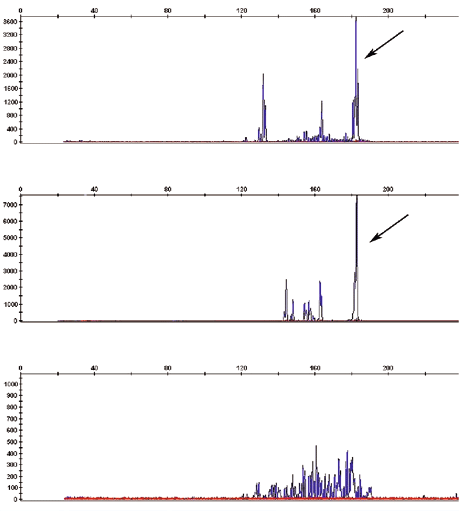
Выявление моноклональности по генам TCRγ методом фрагментного анализа у пациента с грибовидным микозом IIА степени. В крови и биоптате кожи, морфологически соответствующей бляшке, выявляются одинаковые моноклональные пики (указаны стрелками). В биоптате кожи, морфологически соответствующей пятну, — поликлональная картина: а — образец периферической крови; б — биоптат кожи (бляшка); в — биоптат кожи (пятно)
Полученные данные свидетельствуют о корреляции между гистологически подтвержденными диагнозами ТКЛК и ВКЛК и выявлением моноклональности лимфоцитов по генам γ- и β-цепей TCR, а также по генам тяжелых цепей Ig соответственно, что дает основание использовать данные молекулярно-генетические методы с помощью ПЦР в ранней диагностике ЗЛК.
Кроме того, были подтверждены данные зарубежных исследователей о том, что моноклональность при ТКЛК развивается по мере нарастания инфильтративных изменений в очаге поражения. Обнаружение клона лимфоцитов в образце крови, идентичном биоптату кожи, свидетельствует о рециркуляции его из очага пораженной кожи в периферическую кровь.
Литература
1. Assaf C., Hummel M., Dippel E. et al. High detection rate of T-cell receptor beta chain rearrangements
in T-cell lymphoproliferations by family specific polymerase chain reaction in combination with the GeneScan technique and DNAsequencing. Blood 2000; 96(2): 640—646.
2. Simon M., Kind P., Kaudewitz P. et al. Automated High-Resolution Polymerase Chain Reaction Fragment Analysis. Am J Pathol 1998; 152: 29—33.
3. Holm N., Flaig M. J., Yazdi A.S. et al. The value of molecular analysis by PCR in the diagnosis of cutaneous lymphocytic infiltrates. J Cutan Pathol 2002; 29: 447—452.
4. Furmanczyk P.S., Wolgamot G.M., Kussick S.J. et al. Diagnosis of mycosis fungoides with different algorithmic approaches. J Cutan Pathol 2010; 37: 8—14.
5. Никитин Е.А., Сидорова Ю.В., Рыжикова Н.В. и др. Определение Т-клеточной клональности по гамма-цепи Т-клеточного рецептора: окончательные данные. Терапевтический архив 2006; 7: 52—57.
6. Muche J.M., Lukowsky A., Ahnhudt C. et al. Peripheral blood T cell clonality in mycosis fungoides -an independent prognostic marker? J Invest Dermatol 2001; 116 (3): 484—485.
7. Selkuvic K.L., Cikota B., Stojadinovic O., et al. TCRγ gene rearrangement analysis in skin and blood of mycosis fungoides patients. Acta Dermatovenerologica Alpina, Pannonica et Adriatica 2007; 16 (4): 149—155.
8. Cotta A.C., Cintra M.L., Macedo de Souza E., Magna L.A., Vassallo J. Reassessment of diagnostic criteria in cutaneous lymphocytic infiltrates. Sao Paulo Medical Journal 2004; 122 (4): 161—165.
9. Delfau-Larue M.H., Laroche L., Wechsler J. et al. Diagnostic value of dominant T-cell clones in peripheral blood in 363 patients presenting consecutively with a clinical suspicion of cutaneous lymphoma. Blood 2000; 96 (9): 2987—2992.
10. Dippel E., Assaf C., Hummel M., et al. Clonal Tcell receptor gamma-chain gene rearrangement by PCR-based GeneScan analysis in advanced cutaneous T-cell lymphoma: a critical evaluation. J Pathol 1999; 188: 146.
11. Klemke C.D., Dippel E., Dembinski A. et al. Clonal T cell receptor gamma-chain gene rearrangement by PCR-based GeneScan analysis in the skin and blood of patients with parapsoriasis and early-stage mycosis fungoides. J
Pathol 2002; 197 (3): 348—354.
12. Callan M.F., Steven N., Krausa P. et al. Large clonal expansions of CD8+ T cells in acute infectious mononucleosis. Natural Medicine 1996; 2(8): 906—911.
13. Lee S.C., Berg K.D., Racke F.K. et al. Pseudo-Spikes Are Common in Histologically Benign Lymphoid Tissues. J Mol Diagn 2000; 2 (3): 145—152.
14. Botella-Estrada R., Sanmartin O., Oliver V. et al. Erythroderma. A clinicopathological study of 56 cases. Archives of Dermatology 1994; 130: 1503.
8. Cotta A.C., Cintra M.L., Macedo de Souza E., Magna L.A., Vassallo J. Reassessment of diagnostic criteria in cutaneous lymphocytic infiltrates. Sao Paulo Medical Journal 2004; 122 (4): 161—165.
9. Delfau-Larue M.H., Laroche L., Wechsler J. et al. Diagnostic value of dominant T-cell clones in peripheral blood in 363 patients presenting consecutively with a clinical suspicion of cutaneous lymphoma. Blood 2000; 96 (9): 2987—2992.
10. Dippel E., Assaf C., Hummel M., et al. Clonal Tcell receptor gamma-chain gene rearrangement by PCR-based GeneScan analysis in advanced cutaneous T-cell lymphoma: a critical evaluation. J Pathol 1999; 188: 146.
11. Klemke C.D., Dippel E., Dembinski A. et al. Clonal T cell receptor gamma-chain gene rearrangement by PCR-based GeneScan analysis in the skin and blood of patients with parapsoriasis and early-stage mycosis fungoides. J
Pathol 2002; 197 (3): 348—354.
12. Callan M.F., Steven N., Krausa P. et al. Large clonal expansions of CD8+ T cells in acute infectious mononucleosis. Natural Medicine 1996; 2(8): 906—911.
13. Lee S.C., Berg K.D., Racke F.K. et al. Pseudo-Spikes Are Common in Histologically Benign Lymphoid Tissues. J Mol Diagn 2000; 2 (3): 145—152.
14. Botella-Estrada R., Sanmartin O., Oliver V. et al. Erythroderma. A clinicopathological study of 56 cases. Archives of Dermatology 1994; 130: 1503.
15. Cherny S., Mraz S., Su L., Harvell J., Kohler S. Heteroduplex analysis of T-cell receptor g gene rearrangement as an adjuvant diagnostic tool in skin biopsies for erythroderma. J Cutan Pathol 2001; 28: 351—355.
16. Beylot-Barry M., Sibaud V., Thiebaut R., et al. Evidence that an identical T cell clone in skin and peripheral blood lymphocytes is an independent prognostic factor in primary cutaneous T cell lymphomas. J Invest Dermatol 2001; 117 (4): 920—926.
17. Willemze R., Jaffe E.S., Burg G., Cerroni L., et al. WHO-EORTC classification for cutaneous lymphomas. Blood 2005; 105: 3768—3785.
18. Dongen J.J., Langerak A.W., Bruggemann M. et al. Design and standardization of PCR primers and protocols for detection of clonal immunoglobulin and T-cell receptor gene recombinations in suspect lymphoproliferations:
report of the BIOMED-2 Concerted Action BMH4-CT98-3936. Leukemia 2003; 17: 2257—2317.
19. Greiner T.C., Raffeld M., Lutz C. et al. Analysis of T-cell receptor-gamma gene rearrangements by denaturing gradient gel electrophoresis of GC-clamped polymerase chain reaction products: correlation with tumor-specific sequences. Am J Pathol 1995; 146: 46—55.